遠隔患者モニタリングによる血圧管理のための測定時間帯自動分析機能の開発
脳・心血管病予防のためには血圧管理が重要であるが、十分徹底されておらず世界的な社会課題となっている。米国においても官民により様々な取組が実施されてきたが、2019年世界に先駆けて遠隔患者モニタリングを保険償還の対象に定めた。この動きに呼応して、オムロンヘルスケアでも遠隔患者モニタリングシステムVitalSightTMを提供している。電子カルテに家庭血圧を直接送信する提供形態の場合、大量の測定結果が医療者に多くの負荷をかけるという課題が生じた。このためいくつかの解決手法を提案しているが、本論文では、医療者の負荷を増やさずに各個人に適した朝晩血圧表示をするための、測定時間帯自動分析機能の開発・評価結果を報告する。同機能は、個人別に単位時間毎の測定頻度を集計し、毎日の測定習慣を特定する。実際に電子カルテに送信された測定結果を用いて検証し、同機能にて個人別に測定している時間帯を判別できることを確認した。この機能を用いて朝晩血圧グラフを表示すれば、医療者が薬の効果を容易に判断できる、また症状を示唆する普段と異なる測定時間を発見できることが期待され、臨床有用性が確認されることが望まれる。
1. まえがき
1.1 血圧管理とモニタリングの必要性
世界中で多くの高血圧患者が目標となる血圧値に管理されていない1)。米国においても、国民の半数が高血圧にり患しているが、目標血圧値まで降圧されている患者は、わずかその4分の1である。さらにそれは年間約50万人の死因となっており、年間1310億ドルの医療費が必要となっている。これらを米国政府は認識し、医療従事者に血圧管理を強化するよう声明を出している2)。高血圧治療による降圧目標値達成率の向上は、改善が必要な社会課題となっている。
2012年、米国疾病コントロールセンター(CDC)と米国政府管掌保険であるメディケアメディケイド(CMS)は、心血管イベントを削減することを目的としてMillion Hearts®というプログラムにより降圧目標値達成率80%を設定し血圧管理のための情報提供を行ってきた3)。
2017年からは米国心臓協会(AHA)と米国医師会(AMA)が、これにTarget: BPTMというプログラムを連携させ募集した各医療機関の患者の血圧をオンラインで収集し、医療機関毎の降圧目標値達成率ランキングを公表、表彰するなどの取り組みを行っている4)。
また、Margolisらは、遠隔医療を用いた血圧のモニタリングと薬剤師による管理によって降圧目標値達成率の改善に取り組み、従来治療群よりも血圧が改善され、さらに長期に改善が維持されることを確認している5)。
1.2 遠隔患者モニタリングサービスの開始
2019年1月CMSは、遠隔生理学的(患者)モニタリング(Remote Physiological Monitoring)への保険償還を開始した6)。これに呼応する形で、オムロンヘルスケア米国販売会社であるOmron Healthcare, Inc.は、2020年8月より家庭で測定した患者の血圧値と体重を医療者に伝えるVitalSightTMサービスを開始した7)。
同サービスは、スマートフォンとの通信技術であるBluetooth® Low Energyに対応した血圧計や体重計を、スマートフォンと同様の通信機能を持つHUBと呼ばれる装置を経由して4G LTE/5G携帯電話網に接続し、測定結果を直接医療者のダッシュボードや電子カルテに表示できるシステムである。あらかじめ通信HUBを機器とペアリングさせ患者へ発送することにより、スマートフォンを持っていない、あるいは使い慣れていない患者でも利用できるほか、ペアリング操作など技術的な問題も回避することができる。さらに測定値が電子カルテに自動転送されることにより、医療者も他の検査結果と同様に容易に活用できることが期待された。
Northwestern大学では、電子カルテを通して観察研究を行い、高血圧患者が同システムを活用して治療され、降圧目標値達成率が向上することを確認した8-10)。
1.3 これまでのオムロンヘルスケアの取り組み
オムロンヘルスケアでは、医療機器である自動電子血圧計を50年以上に渡り製造販売してきた。産官学協力のもと、安心して利用できるよう血圧計の測定精度の向上に努め、高血圧治療の発展にメーカーの立場で貢献してきた。
1994年には、家庭で測定したデータを電話回線で病院の管理用サーバーに転送するホームドックを開始するなど、家庭血圧を収集・活用する取り組みを幾度となく行い、血圧管理の発展にも貢献してきた。
その中でも2012年から2019年には日本において血圧分析サービスMedical LINKを提供し、3G携帯電話網に直接送信できる血圧計を用いて患者の家庭血圧を分析し、高血圧治療に役立てて頂くよう医療者に提示していた11)。
近年は世界各国で個人向けに血圧等のバイタルデータを収集・保存するOMRON Connectサービスを提供しており、一部の国では、それによる測定記録を医療者に提示するHealth data Monitoring System(HMS)のサービスも行っている。
1.4 遠隔患者モニタリングの普及促進のために
以上より、高血圧治療において血圧管理とモニタリングが重要であり、遠隔患者モニタリングが効果的であることが確認できた。そこで、脳・心血管の発症ゼロ(イベントゼロ)を掲げる当社として、より広く普及させることを目的に検討を行った。
まず、医療者へのヒアリングや共同研究によるデータの分析を行い、そこから見えてくる課題と打ち手について検討した。いくつかの検討を行った打ち手のうち朝と晩に分けて血圧の平均値を求める手法は、リスクの高い早朝高血圧を検出する、また降圧薬を服用する時間を決めるために使われている6)が、今回さらなる課題に直面した。そこで、本論文では、この家庭血圧の分析手法のひとつである、朝晩血圧表示の改良について検討を行ったので報告する。
2. 課題と解決手段の提案
2.1 電子カルテにあふれる家庭血圧
遠隔患者モニタリングを用いて電子カルテに直接血圧値を送信する場合、血圧管理に役立つ一方で、その課題も見えてきた。
電子カルテに送信された血圧値は、フローシートと呼ばれる記録表示領域に一つ一つ追加されていった。医師はこの一つ一つを確認して評価する必要があるほか、投薬の効果を確認する場合には、複数の値の平均値を計算するなどの必要があった。
さらに、予め医師により設定された閾値を超えるか、下回るとそのたびに警報が通知される。このシンプルな警報にも、次のような課題があった。
警報が通知されると、医師や他の医療者は原因を究明するため、患者に連絡する必要があるかその結果が緊急事態を意味するかどうか判断する必要があったが、多くの場合連絡したところ緊急ではないことがわかった。例えば、安静状態でなかったり測定姿勢が適切でなかったりしただけで、普段とは異なる高い値が出ることがあった。
他方、臨床対処が必要な警報が通知された場合でも、降圧薬の処方量を増やすなどの対応後、薬の効果により血圧が安定するまでの間は警報が通知され続けることになる。
警報が通知された際に医師が時間を取って確認をしても、対処が不要であれば他の患者への対処が遅れるなど不合理である。一方で、警報を無視してしまうと、本来対処が必要であった場合に見落としの責任も生じてしまう。
このため、単純に電子カルテに接続しただけでは、医師の負担が増える、また医師をサポートする医療者がデータを確認しトリアージを行う必要が生じるなど、医療者の負担が増えてしまうという課題が生じる。
2.2 血圧情報の集約提示による医療者負担の削減
電子カルテに大量に送られる日々の家庭血圧に対して医療者の負担を削減するため、これまでいくつか自動化の提案を行ってきた。複数の血圧値を平均して通知する機能やそれらにより警報が通知される前に、患者にテキストメッセージを送り症状がないか自動で問い合わせる自動問診機能、薬を追加したタイミングとその前後の血圧値のトレンドを示し一目で薬が効いているか確認できる薬効評価機能、また血圧を朝晩で個別に平均し表示する朝晩血圧表示機能などである。これらにより、大量の血圧値を効率よく解釈することができるようになり医療者の負担を減らすことができる。
2.3 血圧測定頻度による時間帯別表示
家庭での血圧の分析の際に朝晩に測定された血圧値をそれぞれ分けて平均値を求めることは有益であるが、医療者の負担になるため自動化が望まれる。しかしながら、時間帯を固定してしまう従来法では実際の測定時間帯とずれが生じる。そこで、毎日の血圧測定時間の頻度を算出し、頻度の高い時間帯を“朝”ないし“晩”と、患者別に定義して分析する手法を提案した。以下提案法と呼ぶ。
当社では従来より、午前4時から午前9時59分を“朝”、午後7時から翌日午前1時59分を“晩”とする固定時間で仕分けた測定値を集計しグラフや平均値を表示することを提案していた。以下、この方法を固定時間法と呼ぶ。
しかしながら、この方法では次のような課題があった。
- 固定された時間帯に患者が測定できるかわからないこと。
- 時間帯を外れ除外された測定値が重要な意味を持つ可能性があり、見逃しとなる恐れがあること。
- 高齢者やシフトワーカーについては、いつ起床して就寝しているのか明確でないこと。
- 同じ時間帯が朝晩に分割される可能性があること。(例えば午前午後を分割基準とした場合、正午前後に起床し測定すると起床後の血圧と就寝前の血圧が混在する。)
米国のガイドラインにおいては、家庭血圧の測定法として次の通り記載されている。“服薬前の朝と夕食前の晩に、少なくとも2回、1分の間隔をおいて測定すること”12)。
患者の生活時間帯にはある程度の規則性があると仮定し、患者が医療者からガイドラインに従って測定するように指示を受けている場合、毎日おおよそ同じ時間帯に測定されることが期待される。すなわち、血圧を測定する頻度の高い時間帯が存在すると考えられるため、提案法の成立が期待される。
3. 方法
3.1 算出アルゴリズム
提案法では、個々の患者の時間帯別測定頻度を分析し、抽出される頻度の高い時間帯を“朝”、“晩”と定め、それ以外の時間帯を、“その他”として分類する。
このフローチャートを図1に示す。
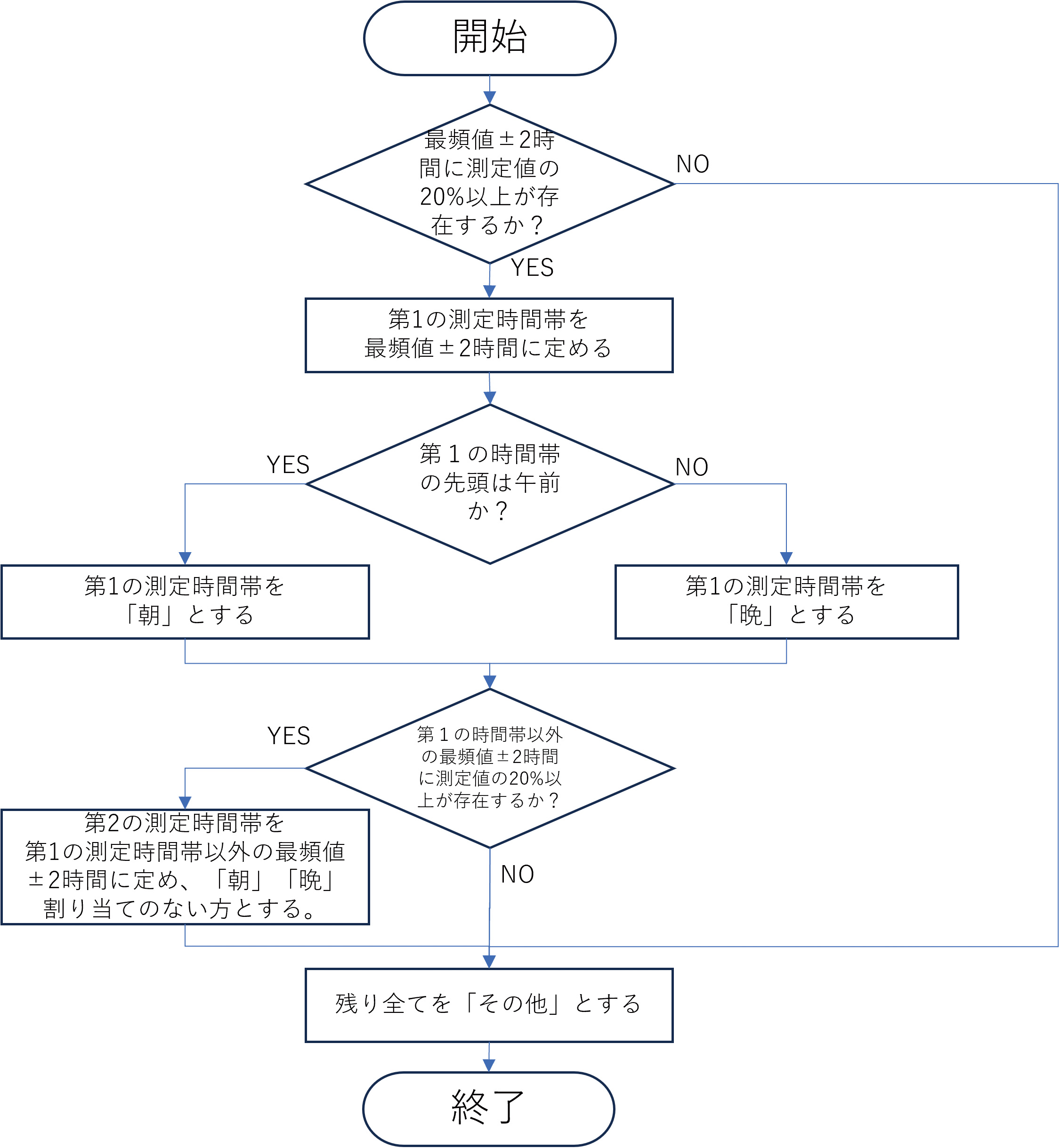
主要なルールを以下に示す。
- ① 頻度は、式(1)に基づいて隣接する頻度の加重平均を用いる。
-
k:時間帯番号[無次元]
wp[k]:加重平均測定頻度[度数]
p[k]:測定頻度[度数] - ② 最も頻度の高い時間を含む時間帯を第1の時間帯、この時間帯以外の次に頻度の高い時間を含む時間帯を第2の時間帯、それ以外の時間帯をその他の時間帯とする。ただし、全体の20%以上の測定値を含むこと。
- ③ 第1、第2の時間帯の幅は±2時間とした。
- ④ 第1の時間帯、第2の時間帯、それぞれの開始時間帯が、一日のうちでいずれか早い方を“朝”とする。ただし、第1の時間帯しかなく、午後であれば、“晩”とする。
- ⑤ 第1の時間帯、第2の時間帯、共に開始時刻が属する日とする。終了時刻が翌日深夜となっても、当日の扱いとする。
- ⑥ 各時間帯を1時間以内で前後にシフトさせた場合に頻度の合計が大きくなる場合はそちらを選択することとする。
※下線部のパラメーターは調整の余地があり、患者背景等による最適化は行っていない。
3.2 検証方法
固定時間法と提案法を実在の測定結果に適用し、“朝”、“晩”、“その他”にそれぞれ分類された個人別の割合を算出し、群毎に再度それぞれの平均値を算出した上で、測定頻度の割合を比較する。個人別に適切に時間帯を選択することができれば、全体においても“その他”の測定頻度の平均値が減少する。従って、“その他”の時間帯の頻度を比較し、従来法よりも提案法において減少していることを成功条件とする。
3.3 データセット
A群 高齢のプライマリケア患者
2020年11月28日から2021年8月14日までの間に、Northwestern Medicine(米国イリノイ州シカゴ)のプライマリケア診療所で高血圧症またはその他の関連適応症に対してVitalSightTMを処方された288人の高齢患者(65歳以上)のうち、血圧値を送信した238名の測定結果を電子カルテから抽出した。
B群 高血圧合併症のある中高年患者
2024年2月8日から2025年1月31日までNorthwestern Medicine(米国イリノイ州シカゴ)で実施されたパイロットスタディに参加した、脳卒中の既往や、心血管疾患、腎疾患、糖尿病等を患う高血圧患者70名のうち、VitalSightTMを用いて血圧値を送信した69名の測定結果を電子カルテから抽出した。なお、測定回数が少ないと朝晩2回ずつ測定するようテキストメッセージが届く設定となっていた。
なお、これらのデータセットの研究での使用は、Northwestern University の倫理委員会及びNorthwestern Medicineのデータ管理者より承認され、HIPAA等の米国の法令や規則に従い、匿名化の上共有されている。
4. 結果
4.1 測定時間帯の分布
検証を行う前に、両群の全測定時間帯分布を確認した。図2、3はそれぞれA群、B群の全測定について、個人を特定せずに、1時間毎の測定回数の分布をヒストグラムで表したものである。朝晩にピークがあるが、深夜早朝昼間など測定時間帯が広く分布していることがわかる。
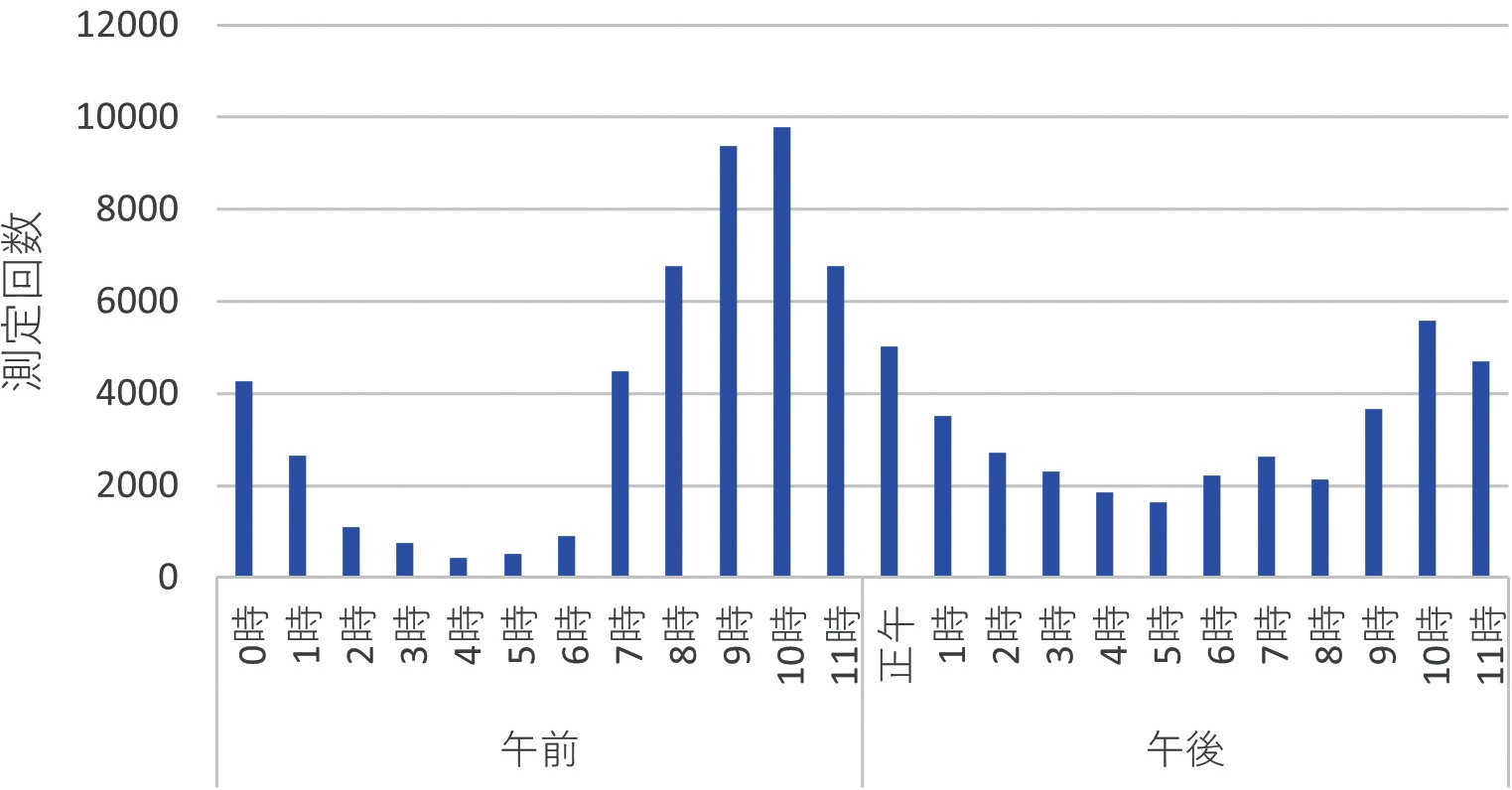
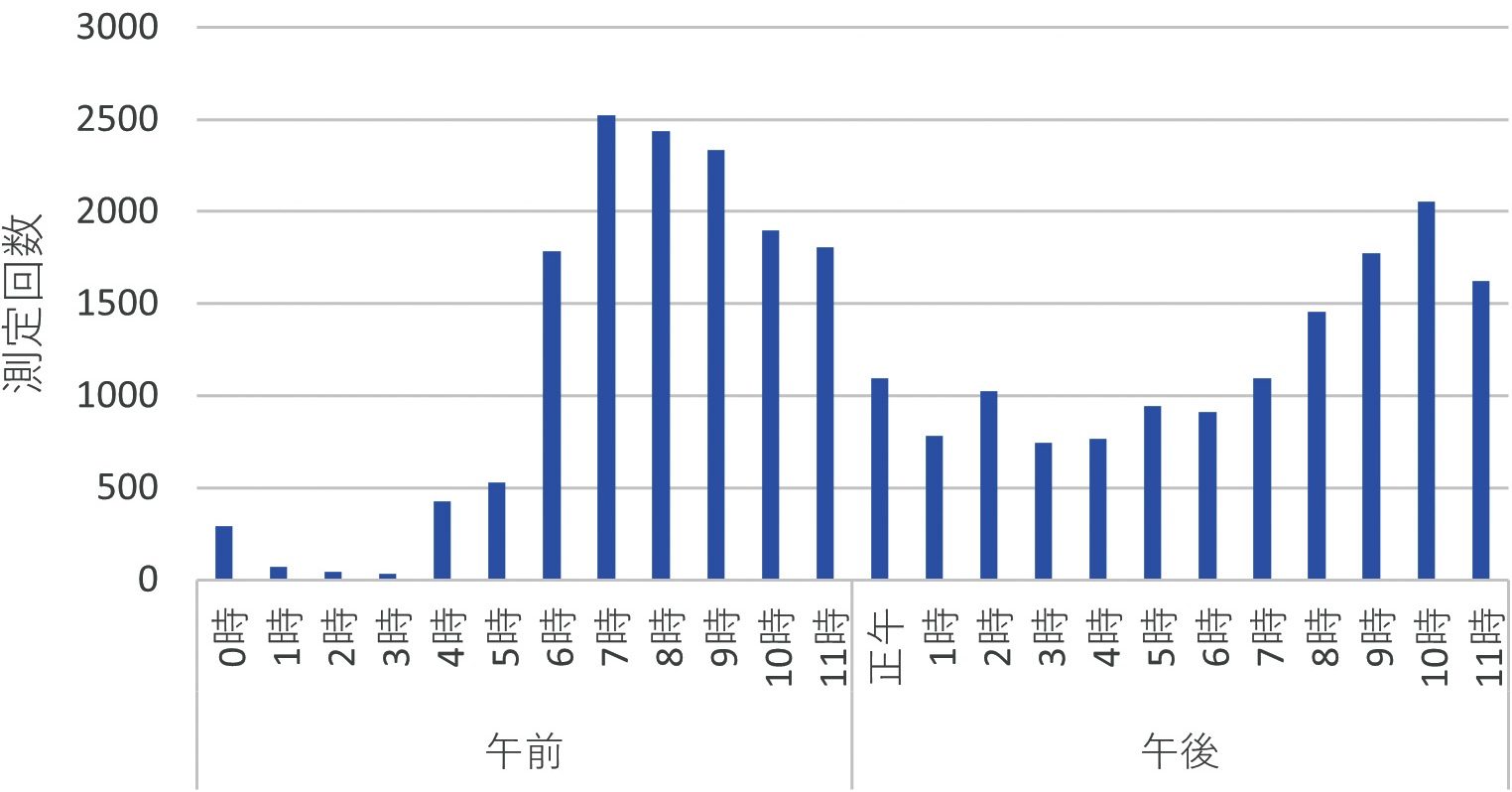
4.2 アルゴリズムの適用
まず、A群、B群、それぞれのデータに対して、提案法を適用しそれぞれ高頻度の時間帯が選択されたか確認した。
図4~9は、実際の個人別の時間帯別測定頻度の代表的なヒストグラムである。横軸は15分単位で頻度を縦軸で示している。
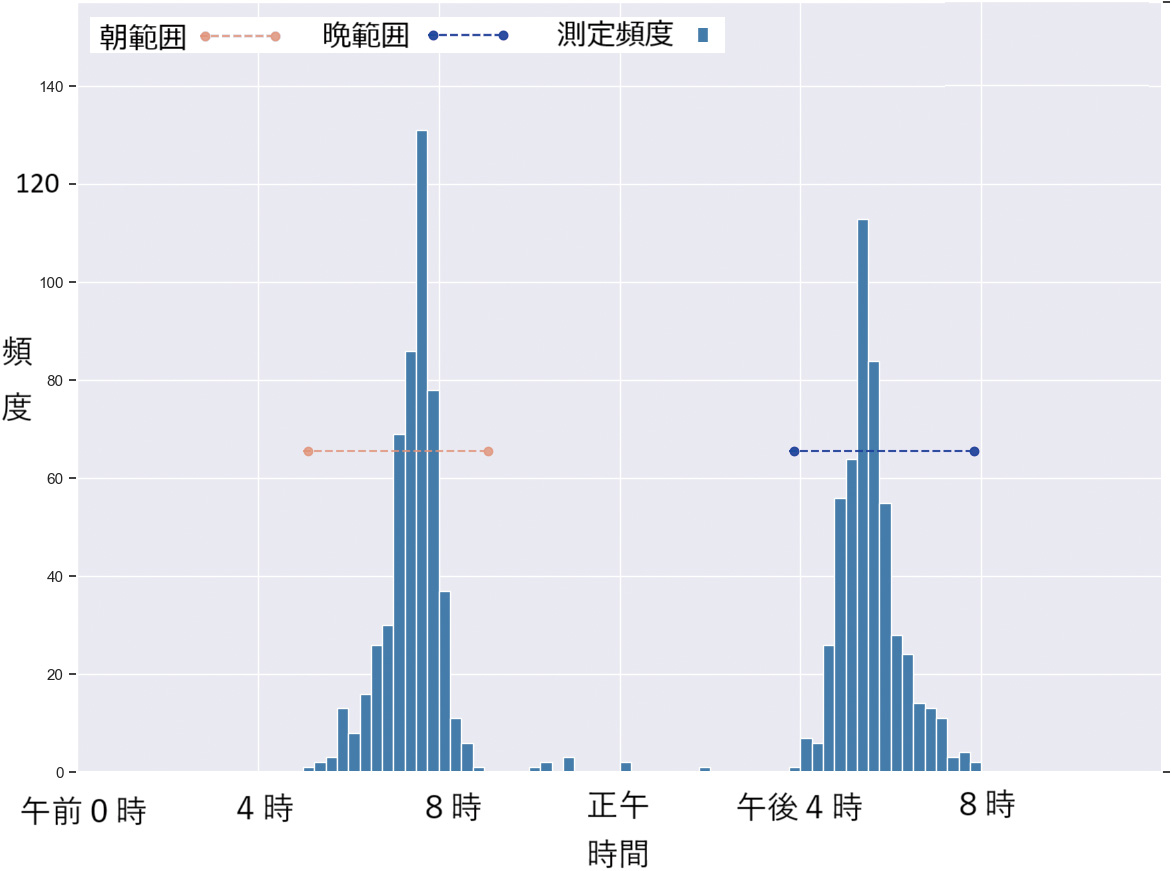
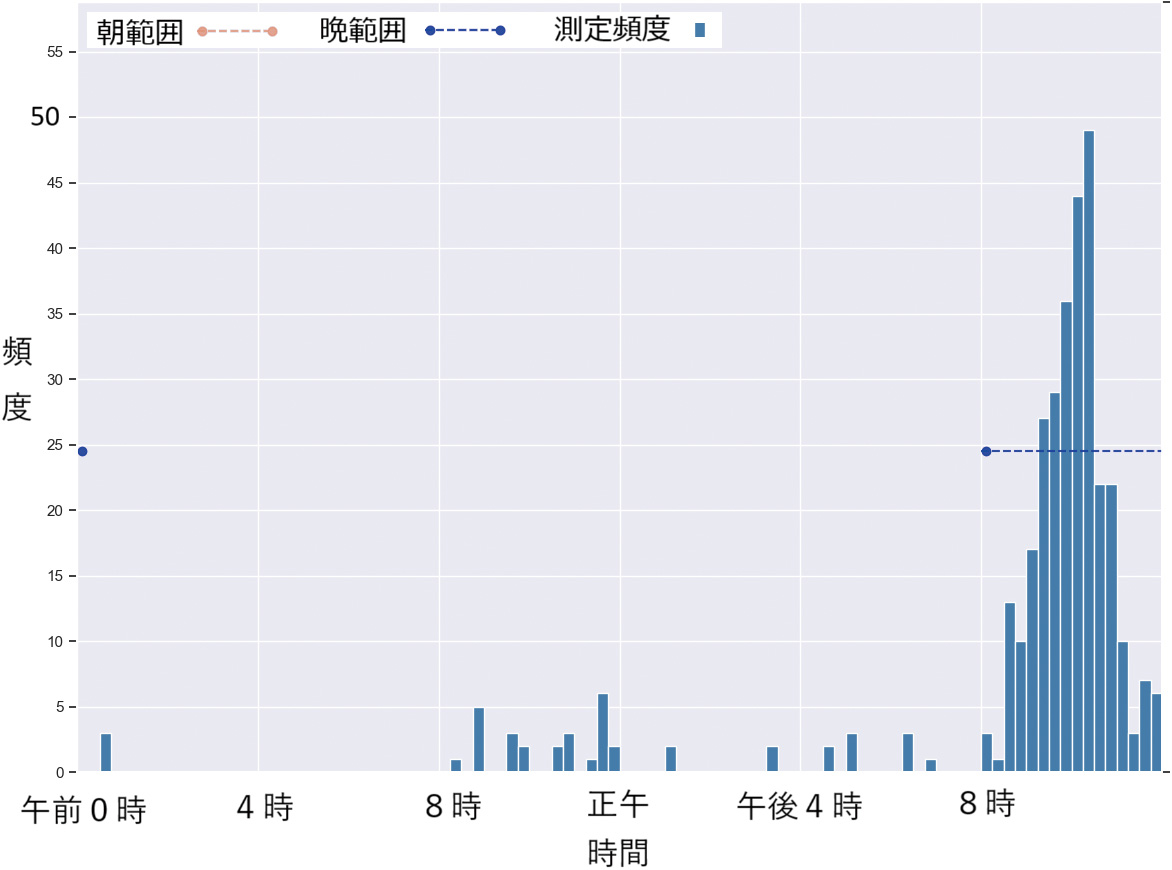
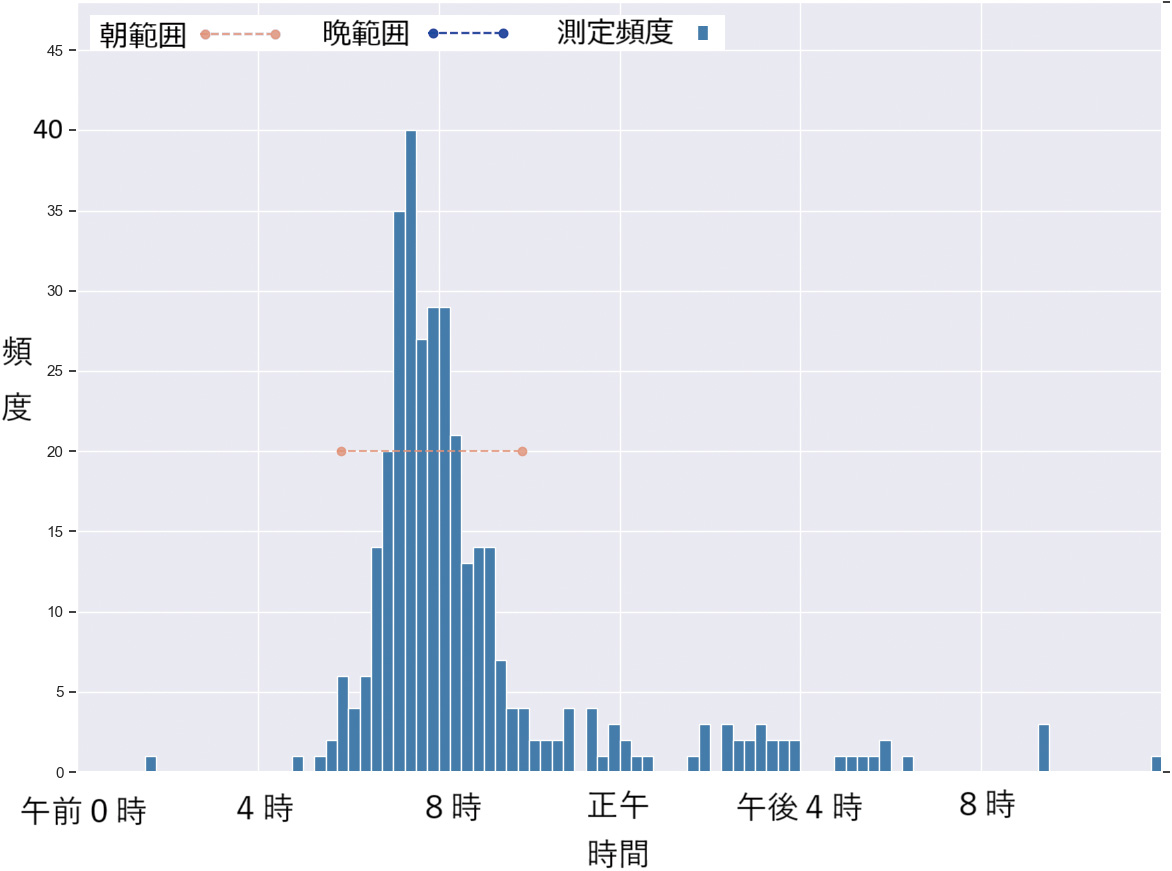
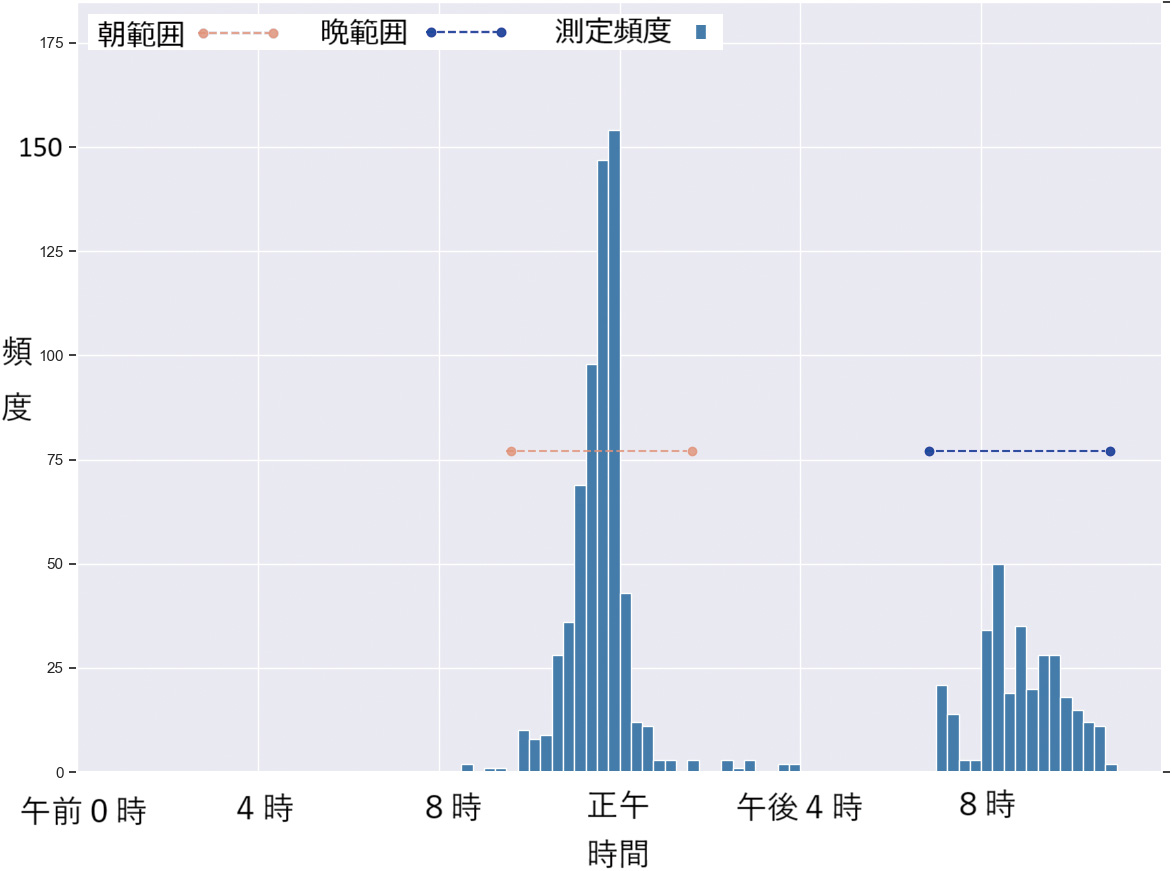
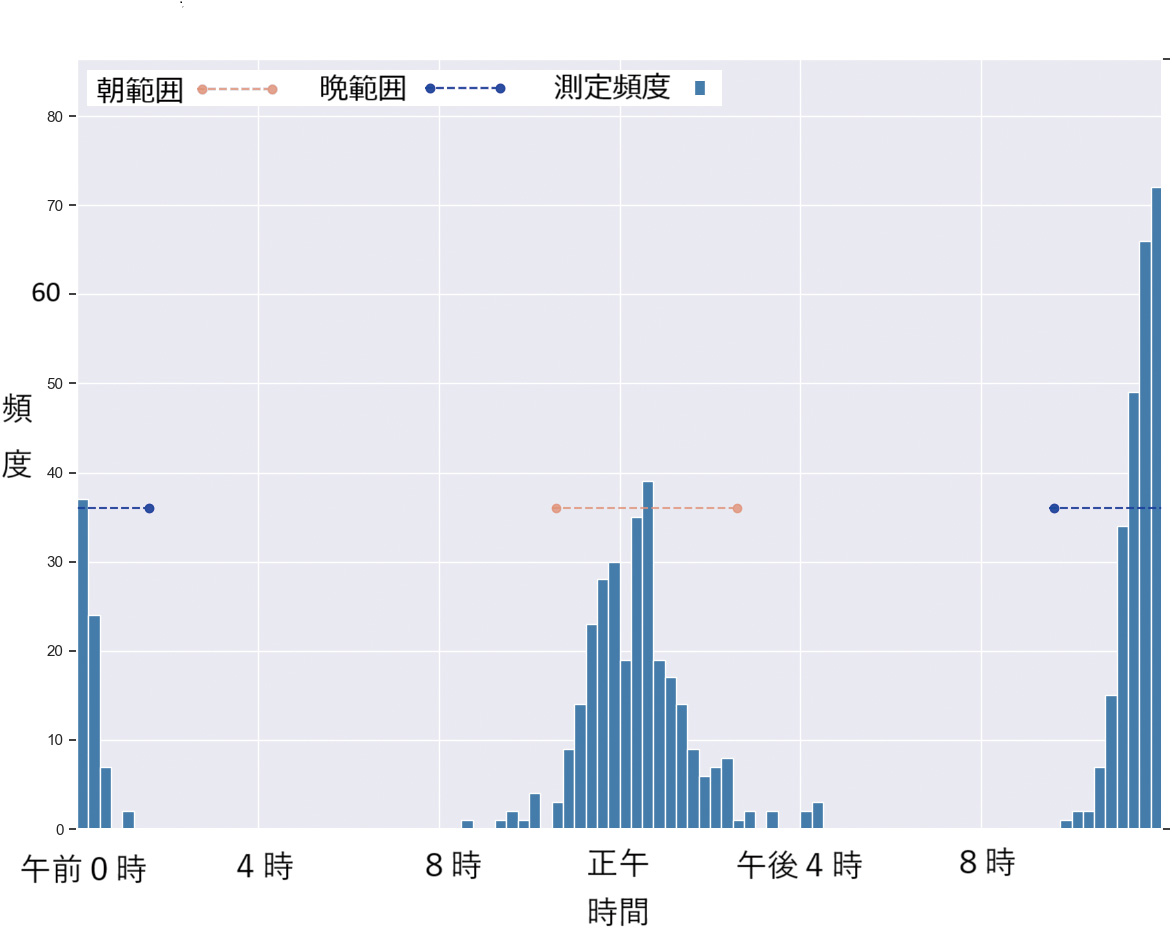
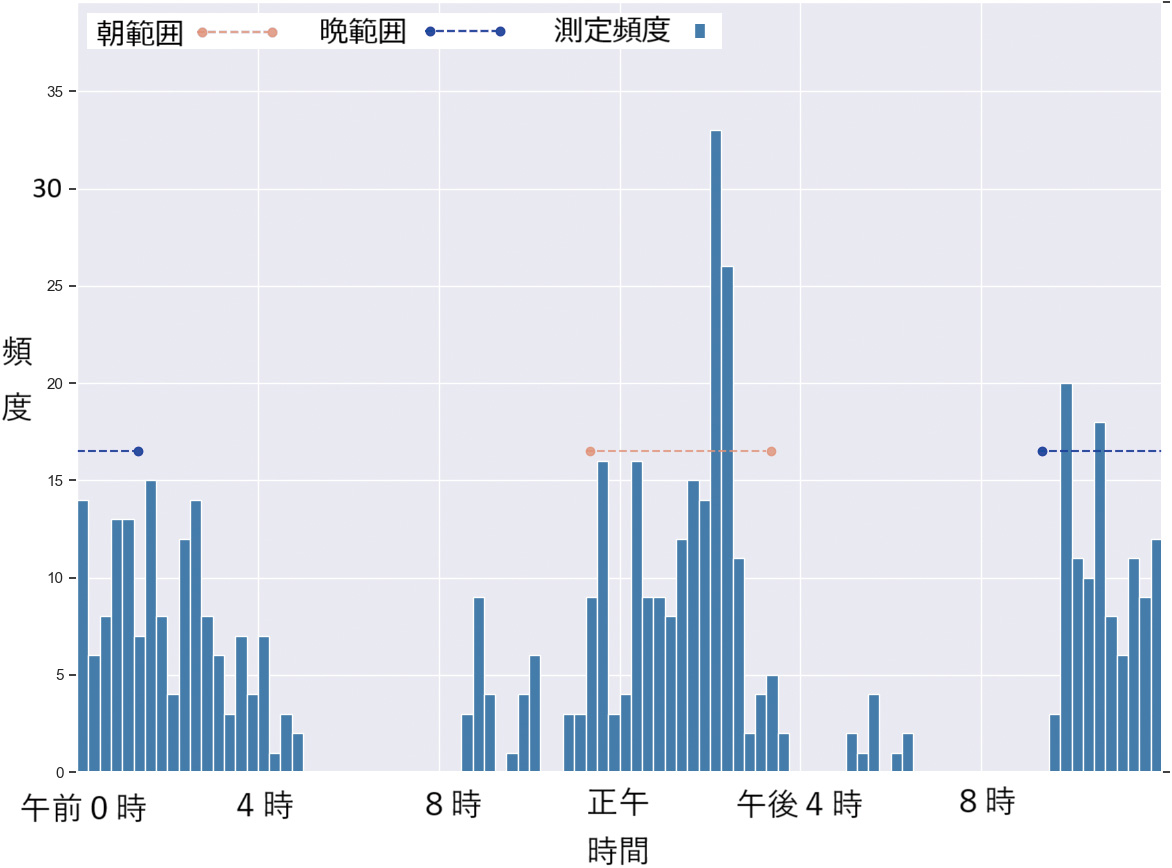
また、提案法により“朝”と判断された時間帯を赤色で、“晩”と判断した時間帯を青色で、両端が丸印の破線により表している。
図4は、朝晩の集中した時間帯に主として測定している被験者の例である。
図5は、晩の集中した時間帯に主として測定している被験者の例である。
図6は、朝の集中した時間帯に主として測定している被験者の例である。
図7は、正午前後と晩の集中した時間帯に主として測定している被験者の例である。
図8は、正午前後と午前0時前後に主として測定している被験者の例である。
図9は、正午過ぎ、深夜に測定しているが、ばらつきが大きい被験者の例である。
正午、深夜0時をまたぐ測定事例について、症例人数をカウントした結果は表1の通りである。2.3で懸念された課題の4が存在していることがわかる。
| 正午をまたぐ人数 (割合) |
深夜0時をまたぐ人数 (割合) |
|
|---|---|---|
| A群 | 123(52%) | 72(30%) |
| B群 | 18(26%) | 10(14%) |
4.3 検証結果
表2、3は、提案法をそれぞれA群、B群へ適用し、個人別の時間帯別に分離された割合をさらに群毎にそれぞれ平均したものである。これらの表の通り両群において提案法では、固定時間法では“その他”に分離され除外されていた測定結果がより多く“朝”“晩”に分離され、“その他”に分類される測定結果が減少し、両群ともにウィルコクソン順位和検定により有意差が確認された。この結果から、提案法では固定時間法に比して、測定結果をより個人別の時間帯に分離できていることがわかる。
| 朝に分離された割合の平均 | 晩に分離された割合の平均 | その他に分離された割合の平均 | |
|---|---|---|---|
| 固定時間法 | 24% | 26% | 50% |
| 提案法 | 52% | 26% | 22% |
| 朝に分離された割合の平均 | 晩に分離された割合の平均 | その他に分離された割合の平均 | |
|---|---|---|---|
| 固定時間法 | 37% | 28% | 36% |
| 提案法 | 46% | 31% | 23% |
4.4 考察
遠隔モニタリングに参加した米国人患者は、1日のうち2つの異なる時間帯に集中して測定をした患者が多くいたものの、測定のタイミングについては患者間で統一性がなかった。A群のピークは午前9時、B群のピークは午前7時だが、B群に比して、A群はやや先鋭である。年齢や群の違いでも、生活時間帯が異なることが示唆されている。また、それぞれ午前10時から午後6時までの測定も多い。
そのため、固定時間法で分析すると中には分析可能な患者もいるものの、それ以外の患者では固定時間以外の測定結果が失われる懸念が生じる。
さらに、正午や午前0時を含む測定時間帯がある患者が半数程度存在し、午前と午後に分けて分析をした場合において、“朝”“晩”あるいは、“服薬前”“夕食前”といった意味が測定値から失われてしまい適切ではない。
これらは、薬効評価の観点で問題となるだけでなく、服薬時刻を検討する際にも誤った判断につながると考えられる。
提案法であれば、個人別の測定パターンを検出できていると同時に、“朝”“晩”に分類されている測定値も固定時間法より増えていることから、期待した効果が得られていると考えられる。
また、個人別の時間帯を分析するためには複数日~数週間の測定が必要であるが、薬効評価等のために測定値を評価する場合は少なくとも2機会以上、3日から1週間の平均値を用いるため問題ないと考えられる。
なお、図9の事例では、測定時刻のばらつきが多いため、各時間帯に含まれているべき測定値がはみ出しているとも言える。これは、3.1で示したパラメーターの調整により、時間帯の幅を広げたり、個人別に調整したりする方法も提案する必要があるかもしれない。一方で、血圧の測定が服薬前に推奨されていることから、測定直後に服薬しているとすれば、服薬時刻がばらついている可能性もあり、測定直後に服薬していない場合は、服薬忘れを助長する可能性もある。血圧の測定及び服薬について時間帯を定め習慣化を奨励する観点からは、測定時刻がゆらぐことは好ましくないとも考えられる。この点については、今後さらなる検討が必要である。
5. 今後の普及に向けて
5.1 提案法により分別表示された血圧の価値
図10は実際の症例から得られた血圧値と脈拍数を、提案法により“朝” “晩” “その他”に分別し週毎の平均を色分けして描画したグラフである。血圧の棒グラフは最上部が最高血圧(収縮期血圧)を表し、最下部が最低血圧(拡張期血圧)を表している。Aは“朝”の血圧値であり、その下への延長線上にある丸印が同時に測定された脈拍数を示している。さらに、Bは“晩”、CとDは“その他”を同様に示している。
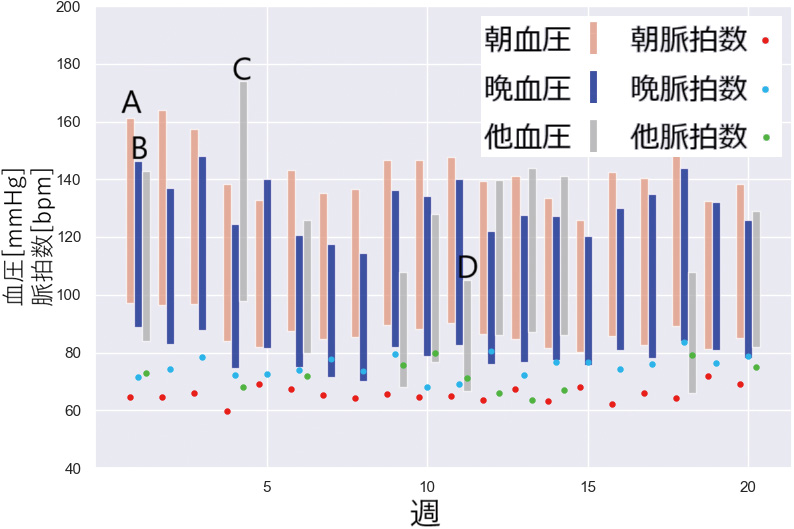
この症例では、当初は血圧が高い状態であったが、上下を繰り返しながら下がってゆくこと、“晩”よりも“朝”が高いことが多いことがわかる。このため、医療者は朝の血圧を下げるように投薬を工夫できることが期待される。
さらに、Cは通常測定時より血圧が高く、Dは血圧が低い状態であり、患者がめまいなど何らかの症状を感じた為、いつもと異なる時刻に測定したと推定される。これにより医療者は、投薬や服薬条件を変える必要があるか検討できる。
図11は別の症例を同様に描画したものである。Eは“朝”の血圧値であり、普段は“朝”のみ血圧値を測定していることがわかる。Fは“その他”の時間帯であり、通常測定時より脈拍数が高い状態であるため、動悸など何らかの症状を感じ、いつもと異なる時刻に測定したと推定される。Gは、同様に通常測定時より血圧が高く、何らかの症状があったものと推定される。これにより医療者は、症状への対処法や頓服の指示などを検討できる。
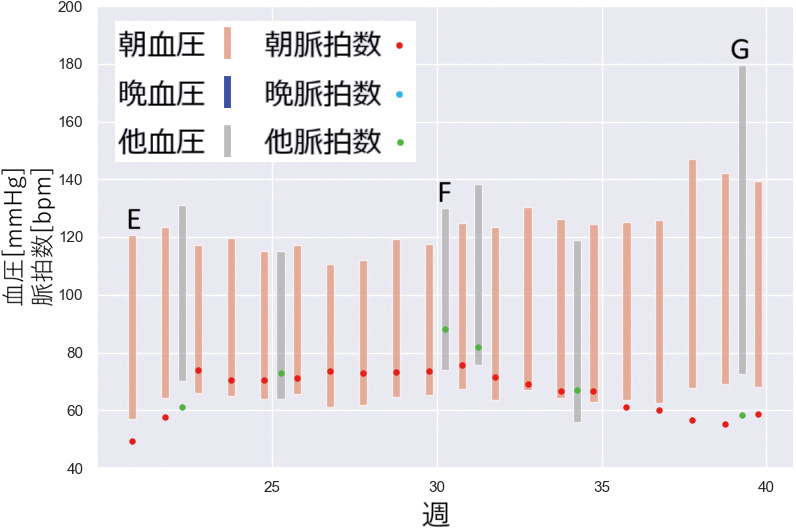
5.2 まとめ
家庭血圧の測定時間帯を認識して時間帯別に平均値を計算することにより、従来法における次の4つの課題を解決し、患者別に通常の生活における“朝”“晩”の血圧値を自動的に算出することができた。
- 固定された時間帯に患者が測定できるかわからないこと。
- 時間帯を外れ除外された測定値が重要な意味を持つ可能性があり、見逃しとなる恐れがあること。
- 高齢者やシフトワーカーについては、いつ起床して就寝しているのか明確でないこと。
- 同じ時間帯が朝晩に分割される可能性があること。
患者がガイドラインに従い“朝”“晩”測定するように、医師から指導を受けているならば、この時間帯に測定した値を診断や薬効評価のために活用されるであろう。
また、“その他”の時間帯に測定された値は、めまいや動悸など、患者が症状を感じて通常と異なる時間帯に測定を行っており個別に判断できるであろう。
これにより、医療者が特段の負荷を増やすことなく、容易に薬効の過不足の確認、患者の症状への細やかな対応が可能となることが期待される。
今後これらの機能と効果が、遠隔モニタリング等のシステムで活用され、医療現場に広く受け入れられるためには、臨床評価により有効性が確認される必要がある。
そして、さらなる課題を深堀、解決策を提案し、高血圧治療と心血管疾患の発症予防に貢献してゆきたいと考える。
共同研究者であり、VitalSightTMの臨床評価等の研究を運営し、今回そのデータを提供していただいた、Feinberg School of Medicine, Northwestern University の、Stephen D. Persell博士、Lucia Petito博士、Yaw Peprah氏、Ji Young Lee氏の諸氏に感謝します。
参考文献
- 1)
- E. Harris, “Majority of people live with uncontrolled hypertension worldwide,” JAMA, vol. 330, no. 16, p. 1515, 2023.
- 2)
- U.S. Department of Health and Human Services. “The Surgeon General’s Call to Action to Control Hypertension.” US Department of Health and Human Services /Enhancing the health and well-being of all Americans. https://www.hhs.gov/sites/default/files/call-to-action-to-control-hypertension.pdf(Accessed: Feb. 12, 2025).
- 3)
- H. K. Wall, et al., “Improving blood pressure control in the United States: At the Heart of Million Hearts 2027,” Am. J. Hypertens., vol. 36, no. 8, pp. 462-465, 2023.
- 4)
- A. P. Smith, et al., “Target: BPTM: A national initiative to improve blood pressure control,” Hypertension, vol. 80, no. 12, pp. 2523-2532, 2023.
- 5)
- K. L. Margolis, et al., “Effect of home blood pressure telemonitoring and pharmacist management on blood pressure control a cluster randomized clinical trial,” JAMA, vol. 310, no. 1, pp. 46-56, 2013.
- 6)
- D. Shimbo, et al., “Self-measured blood pressure monitoring at home a joint policy statement from the American Heart Association and American Medical Association,” Circulation, vol. 142, no. 4, pp. e42-e63, 2020.
- 7)
- 佐藤博則, “高血圧患者の遠隔モニタリングと米国における社会実装,” システム制御情報学会誌, vol. 67, no. 6, pp. 224-229, 2023.
- 8)
- L. C. Petito, et al., “Remote physiological monitoring for hypertension in primary care: a prospective pragmatic pilot study in electronic health records using propensity score matching,” JAMIA Open, vol. 6, no. 1, pp. ooac111, 2023.
- 9)
- S. D. Persell, et al., “Prospective Cohort Study of remote patient monitoring with and without care coordination for hypertension in primary care,” Applied Clinical Informatics, vol. 14, no. 3, pp. 428-438, 2023.
- 10)
- L. C. Petito, et al., “Blood pressure outcomes at 12 months in primary care patients prescribed remote physiological monitoring for hypertension: a prospective cohort study,” J. Hum. Hypertens., vol. 37, no. 12, pp. 1091-1097, 2023.
- 11)
- J. Yatabe, et al., “The current state and future of internet technology-based hypertension management in Japan,” Hypertension Research, vol. 44, pp. 276-285, 2021.
- 12)
- P. K. Whelton, et al., “2017 ACC/ AHA/ AAPA/ ABC/ ACPM/ AGS/ APhA/ ASH/ ASPC/ NMA/ PCNA Guideline for the prevention, detection, evaluation, and management of high blood pressure in adults: a report of the American college of cardiology/American Heart Association task Force on Clinical Practice Guidelines,” Hypertension, vol. 71, no. 6, pp. e13-e115, 2018.
Bluetooth®、Bluetooth Low Energyは、Bluetooth SIG, Inc. USAの商標または登録商標です。
本文に掲載の商品の名称は、各社が商標としている場合があります。














